Bonjour à tous,
Encore une question de génie chimique / chimie industrielle mais je pense que c’est un problème plus de logique en chimie qu’autre chose donc lisez jusqu’à la fin 
Petite explication sur ce qu’est un flash:
En image, un flash c’est ça:
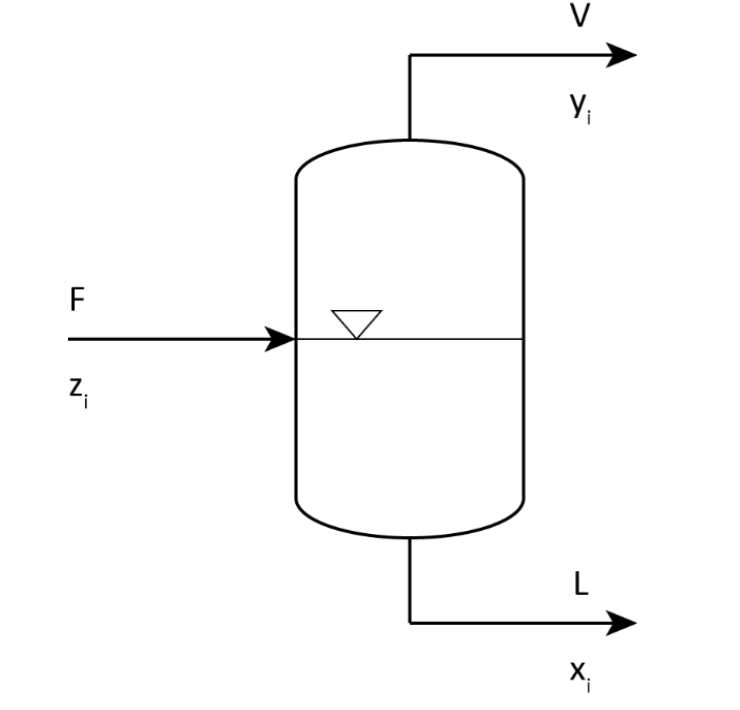
En gros, on a une entrée (débit F en mol/h) composée par exemple de deux espèces A et B avec fractions molaires zA et zB. On fait en gros une distillation et on obtain deux sorties: V et L (qui sont les débit de liquide et vapeur). Dans ces sorties, on a xA et xB qui sont les fractions molaires de A et B en phase liquide. Pareil pour y mais cette fois-ci en phase vapeur.
On peut alors chercher plusieurs choses dont V, L, xA, … en faisant des conservations de masses.
Maintenant, je me demandais d’un point de vue conceptuel si on avait une réaction qui se passerait à l’intérieur. Imaginons on a que du A et B dans F (entrée) qui vont réagir pour former C et D. Disons que la réaction est incomplète et on a encore du A et B à la sortie. On aura donc 4 espèces dans chacune des deux phases.
Le soucis c’est que je vois pas trop comment faire ma conservation de masse. Je pensais écrire Fzi=Lxi+Vyi où i = A, B, C ou D. En assumant qu’on a une solution idéale, on peut appliquer la loi de Raoult yi=Kixi avec Ki la constante de Raoult pour l’espèce i.
Ça donnerait donc (en substituant): xi=[1+(Ki−1)FV]zi
Le soucis c’est que si on prend C par exemple… Eh bien, zC=0 donc xC=yC=0 ce qui ne fait bien sûr pas sens. En fait, c’est comme si je ne prenais pas la réaction en compte mais je vois pas comment je devrais faire :-(
Merci d’avance!

